在继化疗,普通放疗,靶向药物治疗等肿瘤传统治疗后,现如今,免疫疗法已成为肿瘤治疗的技术前沿与中流砥柱,其发展一直倍受关注。与传统化疗放疗不同的是,免疫疗法激活机体自身的免疫系统,利用免疫系统的抗肿瘤作用达到对癌细胞的消灭目的,具有疗效好,副作用小和防止复发等显著优势,可以说革命性地改变了肿瘤治疗的标准与理念,被称为“实验室的奇迹”。
自1986年第一个毛细胞白血病治疗药物IFN-a获批,至今已有约26种肿瘤免疫治疗药物陆续在各国获批,其中肿瘤免疫检查点抑制剂(PD-1,PD-L1,CTLA-4等)、靶向CD3的双抗体、CAR-T细胞免疫治疗都为临床中治疗效果显著的药物,极大地促进了肿瘤治疗市场规模的发展。
溶瘤病毒在最近几十年来在癌症治疗领域一直受到密切关注,研究的不断突破使其成为肿瘤免疫治疗的新秀。2018年7月杜克大学癌症研究所在NEJM上发表的一项研究,利用特殊改造的脊髓灰质炎病毒(一种溶瘤病毒,俗称“小儿麻痹症”)显著延长了胶质母细胞瘤患者的生命,甚至将一位少女完全治愈,再现“实验室的奇迹”,给予医药行业极大鼓舞的同时,也让这种病毒疗法再次走进了大众视野。
溶瘤病毒(OVs)是一类天然的或经过基因改造后可特异性的攻击和破坏癌细胞,而对正常细胞损伤较小的病毒。当然,目前研究的大多是经过基因改造后的病毒,像单纯疱疹病毒、腺病毒、痘病毒等,也有少数天然病毒,如呼肠弧病毒。OVs最早出现的报道,是在1904年,42岁的白血病女患者因为感染了流感病毒而导致了肿瘤的消退,紧接着在1912年,意大利医生发现注射狂犬病毒可引起宫颈癌的消退,由此诞生了溶瘤病毒疗法这一新兴概念,并相关研究迅速进入了狂热期,从1950年到1970年,研究人员开展了大量用野生病毒治疗病毒的临床试验,很快发现,虽然这种病毒疗法的确对肿瘤有一定的抑制作用,但由于无法有效控制病毒的病原性,溶瘤病毒很长时间处于疗法的次要地位,陷入了质疑,直到基因工程技术的出现,让改造病毒基因成为了可能。1991年,胸苷激酶(Thymidinekinase,TK)敲除的基因改造人单纯胞疹病毒I(HSV-1)在小鼠内抑制胶质瘤生长,并且有良好的安全性。1996年,基因改造腺病毒ONYX-015进入I期临床。溶瘤病毒疗法开始慢慢复苏,各项相关研究工作重新迅速展开,2004年,用于治疗黑色素瘤的RIGVIR(非致病性的人肠道细胞病变孤儿病毒)在拉脱维亚获批,成为第一款获监管机构批准的用于癌症治疗的溶瘤病毒药物。2015年10月,FDA批准治疗晚期黑色素瘤的T-vec(单纯疱疹病毒)上市,第二年又分别在欧洲和加拿大获批上市,标志着溶瘤病毒技术的成熟和癌症治疗的认可。
溶瘤病毒相较其它免疫疗法,具有杀伤效率高、成本低,靶向性好、副作用小,具有多种途径杀伤肿瘤,避免耐药性的优势。
由于大部分癌细胞自身抗病毒的机制受损(如多种癌细胞中蛋白激酶R的缺失)与普通细胞相比,病毒更易在癌细胞中复制,杀伤作用也更强,并且病毒的基因组小,对其基因工程的改造较为容易,技术相对成熟,价格成本自然相对低廉。同时正常细胞与癌细胞的很多信号通路和代谢不同(如特有的WNT信号通路),这也是溶瘤病毒疗法的基本原理之一,如成功获批的T-vec,就是敲除了HSV-1的ICP34.5(抑制细胞蛋白的翻译)ICP47(抑制抗原的呈递)这些抑制正常细胞对病毒的清除机制,而癌细胞中缺失这一机制,这样病毒只在癌细胞中复制,有效提高了靶向作用和对患者的安全性。还有目前处于临床3期的Pexa-Vec,就是删除了胸腺苷酸激酶基因,使其只能在高激酶活性的细胞中复制,这一发现具有重大意义,如给肝癌的治疗带来了曙光。
在2000年以前,研究人员大多认为溶瘤病毒对癌细胞的主要杀伤方式是先在肿瘤细胞中繁殖,然后将其裂解,所以溶瘤病毒很长时间一直作为一种单纯的病毒疗法,大部分的研究工作也集中在提高病毒的裂解效率上。而在2000年之后,一些研究人员开始意识到机体免疫在杀伤癌细胞中的重要地位,因为外源病毒的进入,机体免疫对肿瘤和病毒的抗性会有一个偏向性,一般来说,像MHC(主要组织相容性复合体)与病毒抗原的亲和力更高,而且在早期的OVs治疗方案中,弹性病毒引发的免疫倾向于免疫病毒而非癌细胞,但研究发现,使用表达TAA(肿瘤抗原相关蛋白)的复制缺陷型溶瘤病毒进行预处理,可以很好的解决这一问题,使免疫倾向于免疫肿瘤细胞,同时降低了OVs的复制裂解能力,更好的研究机体免疫在OVs疗法中充当的角色。随后的研究发现,OVs杀死癌细胞后,不但会使其释放出TAAs,PAMPs(病原相关分子模式)等,增加了肿瘤抗原的暴露,刺激了机体免疫,并且会感染抗原递呈细胞(APCs)促进其功能的成熟(癌症位点的APC功能常常被破坏),进而导致1型干扰素的应答反应,刺激募集趋化因子(发炎时产生的一种蛋白质,激活白细胞),开始募集T细胞,导致肿瘤特异性免疫应答。一旦被募集后,T细胞开始运输和浸润到肿瘤位点,而OVs可通过多种方式促进T细胞的浸润,例如刺激募集因子产生、诱导炎症刺激因子,甚至可以直接被设计编码T细胞趋化因子,直接解决肿瘤细胞中基因和表观层面上相关基因的缺陷。而一旦这些免疫细胞到达了肿瘤微环境(TME),它们要面临两重困境,一是要克服机体细胞和细胞外基质(ECM)组成的复杂网络,二是要同TME中免疫抑制细胞和其他免疫抑制因子交战,这两个问题OVs都可以提供极大地帮助,首先它可以吸引中性粒细胞,由于中性粒细胞中含有大量的溶酶体酶,可以借助诱导的炎症因子和宿主激酶改变TME,协助免疫细胞穿过ECM,同时OVs可以中和免疫抑制效果,通过诱导强力的促炎Th1(T helper 1)细胞极化免疫应答,显著改变TME,掩护免疫细胞规避免疫抑制。
最后免疫细胞开始与肿瘤细胞交战,往往肿瘤细胞会下调些组分,包括下调抗原形成和呈递的通路来躲避免疫识别,而OVs可以反转这些效果,不但不会使其降低,反而会调高,即便癌细胞自身抗原呈递缺陷,OVs也可增加NK细胞和中性粒细胞的浸润分别通过抗原与MHC机制杀死癌细胞。
综上所述,OVs在机体免疫中可通过增加肿瘤抗原暴露、活化免疫细胞、调节肿瘤微环境、增加肿瘤微环境免疫细胞的浸润等多种途径诱导全身系统的抗肿瘤免疫反应,杀伤肿瘤细胞,实现肿瘤免疫治疗。当然最新的一些研究发现,有些OVs会通过感染肿瘤相关的血管内皮细胞,防止肿瘤血管的形成,从而间接杀死肿瘤细胞。
不同于以往的药物治疗,在耐药性方面,OVs凭借小基因组的优势,可做多种改造,作为载体插入治疗性基因,如细胞死亡相关性分子(P53等)、抗血管生成分子(VEGI等)、免疫调节因子(GM-CSF等)和抑制肿瘤相关基因的小RNA分子(miRNA、siRNA等),很好的避免了耐药性产生。
在肿瘤联合用药领域,OVs疗法由于良好的安全性和多途径的肿瘤杀伤机制,存在着巨大的潜力。目前联合治疗效果显著的是OVs联合免疫检查点抑制剂疗法,人体的免疫检查点网络一般用来抑制免疫诱导的病理反应,即是超敏反应,最大程度上减少对周围正常组织的损伤,而癌细胞通过这一机制,异常上调抑制分子及其相关配体,抑制T细胞活性,避免免疫杀伤。免疫检查点抑制剂的原理则是通过竞争作用解除对T细胞的抑制,达到免疫作用。而在OVs介导的溶瘤过程中,干扰素产物和所募集的T细胞最终会靶向免疫检查点抑制剂(ICIs),限制炎症反应,因此在OVs的使用过程中联合引入ICIs(如PD-1、CTLA4、PD-L1等)能显著提升治疗效果,延长患者的生存期。如2017年7月进入临床3期的T-vec和CTLA4的联合用药对黑色素瘤的治疗几乎有翻倍的效果,而且副作用小。同时,为了减小毒性,OVs还可利用自身“载体”的特性来递送免疫检查点抑制剂,通过改造OVs使其编码ICIs,做到治疗的合二为一。2016年,Kleinpeter及其同事在Oncolmmunology上发表了一项研究结果,用牛痘病毒做骨架编码PD-1,发现感染后的癌细胞和TME中的其他细胞中可以复制产生改造后表达PD-1的病毒,疗效远甚于单剂治疗,但这种分子层面的联和用药的挑战是装载ICIs的OVs要能达到每个解剖学意义上的位点行使功能。
目前,肿瘤免疫治疗方面最火的应该是细胞免疫治疗,如CAR-T(嵌合抗原受体T细胞)细胞疗法,将患者体中取出的T细胞进行改造扩增后,回输入病人体内,所以CAR-T细胞疗法的关键是回输的T细胞的存活率和持久性,这又和T细胞的分化状态有关,宾夕法尼亚大学最近发表的一项研究发现减少CAR-T的体外培养时间可改善对急性白血病的抗性,虽然低分化的细胞是最好的选择,但现实的方案不是研究如何保护T细胞不分化,少分化,而是集中于如何减少CAR-T进入人体后特别在TME中发挥作用时所遇到的障碍,在上文所述中,OVs可以做到调节免疫系统和TME,掩护CAR-T细胞发挥作用,保护其更好增殖,持续在体内运输,并且不仅仅作为一个辅助剂,OVs裂解肿瘤细胞后所放出的TAAs,PAMPs等可进一步引发全身免疫,引起全面T细胞的应答作用。那么,若将CAR-T与OVs联合治疗,其疗效一定甚为可观。但要做到这一步,还需增强目前OVs的系统递送能力,保证其在TME中有更好的传播和持久性。这样,对一些实体瘤的治疗,CAR-T也不再一筹莫展。
溶瘤病毒疗法从1904年发现至今,可谓百年发展,十年突破,爆发在即,相信随着基因改造技术的不断发展,OVs的靶向性,特异性,安全性将逐步提高,在肿瘤联合用药中也将扮演着不可或缺的角色,迎来自己的机遇和癌症完全治愈的希望!
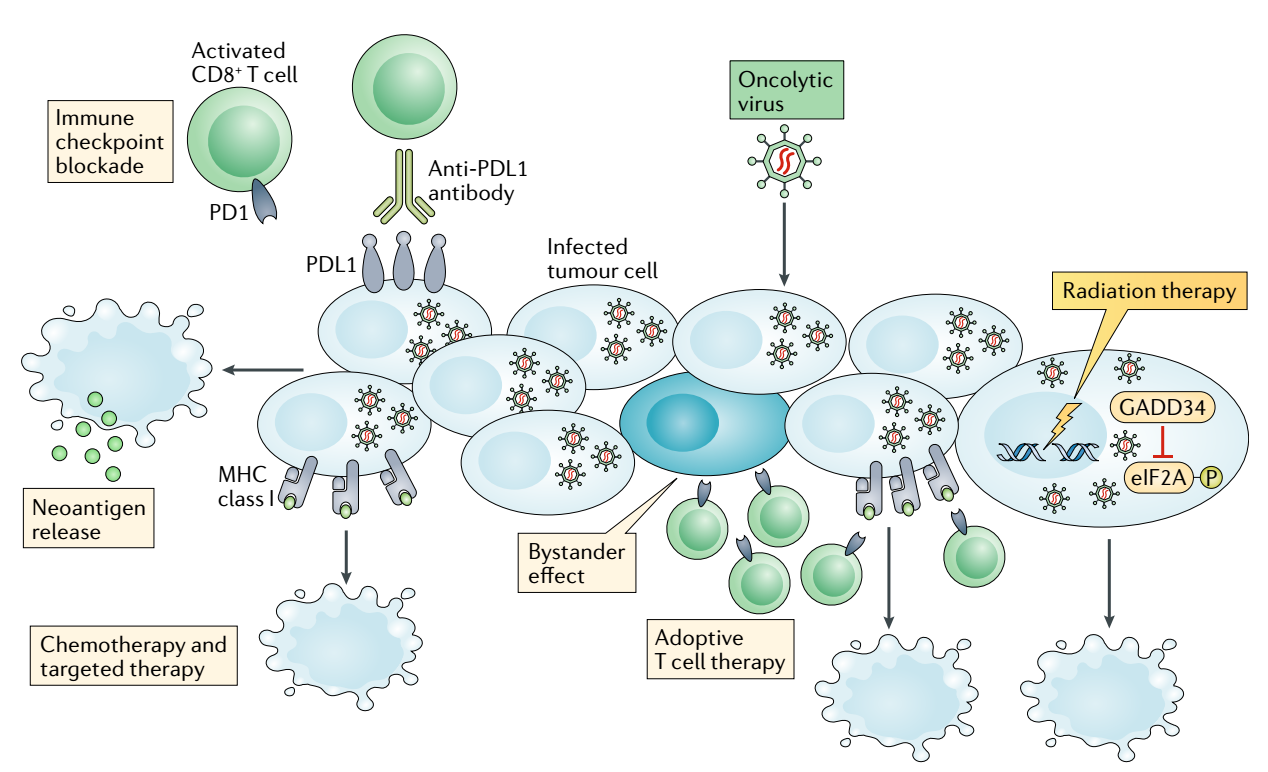
图片来自Nat Rev Immunol

