嵌合抗原受体(CAR)T细胞疗法是通过改造癌症患者的T细胞而构建的、用以识别肿瘤细胞的一种基因工程细胞,它已经在侵袭性的血液肿瘤中证明了其成功,但还没有显示出治疗实体肿瘤的能力。为了克服这个障碍,研究人员通过基因工程技术改造人T细胞,用以产生能够识别在各种癌症细胞都表达的、但不在正常细胞中出现的一种糖肽CAR蛋白,然后证明了其在白血病和胰腺癌小鼠模型中的效力。这一概念性的研究发表于 6月21日的Immunity杂志(影响因子:24.082)。论文标题为“Engineered CAR T Cells Targeting the Cancer-Associated Tn-Glycoform of the Membrane Mucin MUC1 Control Adenocarcinoma”。
该视频显示正常和癌变组织存在MUC1和Tn-MUC1。 A)共聚焦显微镜展示免疫染色的细胞表面蛋白的EpCAM(红色正常人肾)。正常MUC1在人类肾脏细胞表面表达。 B)正常人的肾脏免疫染色的EpCAM和Tn-MUC1(绿色)。 TN-MUC1在正常表达MUC1蛋白的细胞的内部。 C)人乳腺癌免疫染色的EpCAM和Tn-MUC1。 Tn-MUC1在癌症细胞膜表面被发现。
研究者们对T细胞进行基因修饰,让它们靶向区分一种具有截断的糖分子的癌症相关表面蛋白。未来的癌症免疫疗法将T细胞对癌症特异性的糖分子和癌蛋白的靶向区分能力结合起来,可能引起人们为癌症病人开发出一种非常有效的和安全的新疗法。这些经过基因改修饰的T细胞将可以增加这种免疫疗法的癌症特异性和降低对患者的潜在毒性。
在最近的临床试验中,CAR-T细胞疗法已显着改善了晚期且无药可救的血癌患者的治疗效果,如白血病和淋巴瘤。但其用于治疗实体瘤的全部潜力还没有得到开发,因为它们会靶向正常细胞和癌细胞的表面上共有的分子,从而导致严重的副作用。
在一般情况下,CAR-T细胞治疗包括收集病人血液中的T细胞(类似于血液透析的过程)以及通过基因工程技术在这些T细胞表面表达能够识别肿瘤细胞表明特定蛋白的分子。随后这些被修改的T细胞被回输给病人用以定位并且杀死肿瘤细胞。
在此项研究中,论文的第一作者Posey、论文共同通信作Laura Johnson博士(细胞免疫治疗中心,实体肿瘤免疫实验室的负责人)以及来自宾夕法尼亚大学的Carl June和Richard W. Vague教授表示,他们希望快速找到一个切实的解决方案的动机是非常个人化的。他们一个在癌症遗传学领域作出终身贡献的同事被诊断为癌症晚期 。 “她了解我们的工作,并询问是否有任何希望的治疗方法。知道我们有可能能够帮助她,” Johnson说。 “这确实振奋了我们的团队,我们发起全球性的协作,寻找并快速跟踪潜在的能够在临床应用的治疗方法 。”
随着靶向免疫治疗的进行,患者的肿瘤给我们带来了巨大的挑战”我们没有找到任何在其它几种我们正在研究的肿瘤中存在的标志物,” Johnson说。”这是我们在她的肿瘤上发现的唯一的一个标志物;而事实证明,在几乎我们测试过的其它肿瘤中也都发现了这个标志物。”
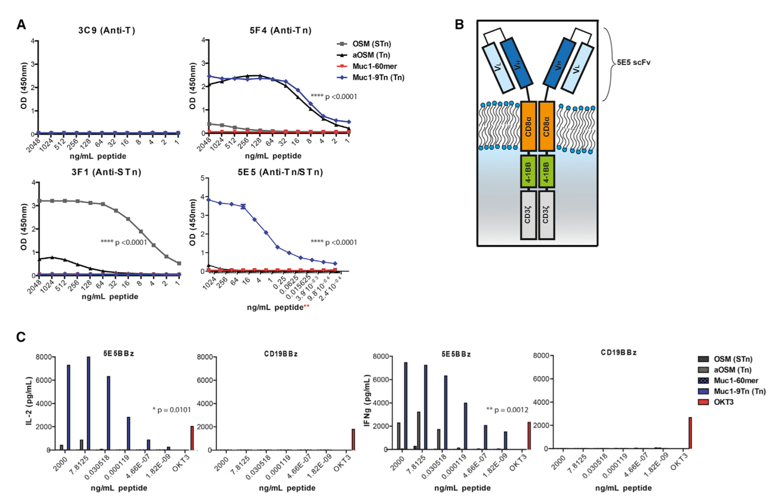
5E5单抗以及5E5CAR特异性识别Tn-MUC1,但是不能单独识别肽
Johnson和她的团队所确定的癌症细胞标志物是一种蛋白质糖基化的特异性变化 。通过与哥本哈根大学和芝加哥大学的研究者合作,科学家小组开发了新型的CAR-T细胞,表达一种叫5E5的单抗,它能够特异性识别一种糖修饰,即mucin 1 (MUC1)蛋白上的Tn多糖,这类修饰不存在于正常细胞,但在癌细胞中非常丰富。简单的说,这是一种靶向癌细胞表面Tn-MUC1(一种新的neoantigen)的新型CAR-T疗法。
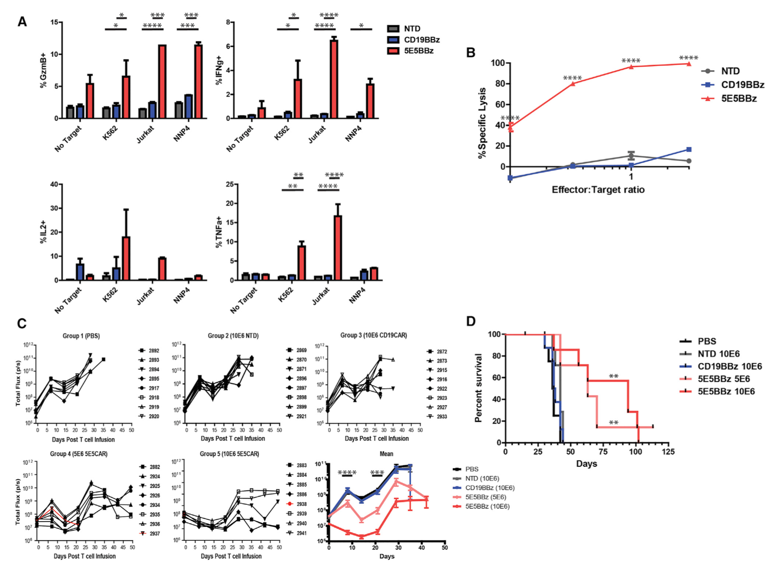
5E5 CAR T 细胞体内/体外抗肿瘤功效
当把这些CAR-T细胞注射回白血病或胰腺癌小鼠体内后,这些肿瘤都萎缩了,而且在大部分小鼠中被消除了,从而引起存活期增加。在接受CAR-T治疗后,胰腺癌小鼠依然活了113天;可是,在接受不可以靶向区分具有截断的糖分子的MUC1蛋白的CAR-T治疗的小鼠当中,在此项实验结束时,仅有三分之一的小鼠存活下来。重要的一点是,这些经过基因修饰的CAR-T不可以伤害正常的人细胞,也不可以伤害不具有这种异常糖分子的细胞。
除此以外,利用高性能显微镜证实正常的细胞仅在细胞内部表达不成熟的癌症相关的MUC1蛋白版本,可是,癌细胞将这种异常的蛋白运送到它的表面上,因而,这有助解释为什么这些经过基因修饰的CAR-T仅可以区分肿瘤细胞表面上的这种癌症特异性的蛋白。
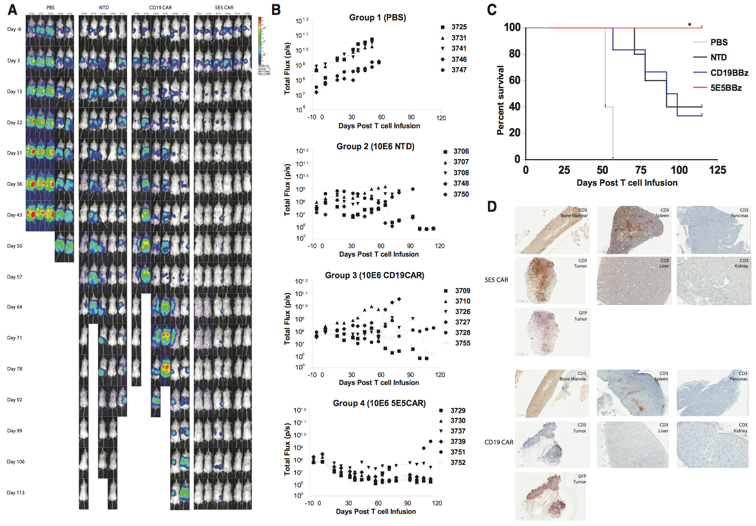
针对弥散性胰腺癌的5E5 CAR-T细胞治疗的小鼠显示出优异的肿瘤排斥和生存时间延长效果
这些发现提示着靶向区分在正常组织和实体瘤中发现的蛋白上存在的异常的癌症特异性糖分子可能成为一种治疗实体瘤的新免疫疗法。这种肿瘤组合区分能力可能引起人们在未来为癌症病人开发出一种安全的有效的疗法。
至于缺点,Johnson称,这是一种非常新的疗法,有很多与肿瘤水平相关的因素可能会限制治疗。接下来,需要做更多的工作来验证这一疗法在晚期小鼠模型中的安全性,因为这才能更准确的预测在人体中的安全性;并需要证明这一疗法对转移性癌症的疗效,因为这类癌症是癌症相关死亡的主要原因。因此虽然我们满怀希望,没有人知道,一个癌症治疗方法是不是真正能够安全且有效,直到它实际应用于临床。
Posey当前正在与哥本哈根大学同事Catharina Steentoft博士合作开发这种类型的新疗法。Johnson说,“我们的研究称这种新的癌症靶向疗法的安全性和有效性。我们正在其他的模型中继续评估这种疗法的安全性。一旦新的模型评估完毕,我们计划将这种疗法推向针对实体瘤病人的I期临床试验当中。遗憾的是,那位女同事已经去世了。”

